ظهور ویروس کووید19 و متعاقب آن، شیوع یکی از کشندهترین بیماریهای همهگیر قرن حاضر، به توسعة فناوریهای پیشرفته برای تشخیص زودهنگام این بیماری منجر شده است. همگرایی هوش مصنوعی و سیستمهای قابل حمل، بهویژه گوشیهای هوشمند، راهحل قانعکنندهای برای تشخیص سریع این بیماری است. هوش مصنوعی بهعنوان روش پذیرفتهشده و رایج، بهتازگی برای تجزیهوتحلیل دادههای بزرگ، نهتنها برای مقابله با بیماری همهگیر کرونا و مدیریت آن، بلکه در زمینههای مختلف پزشکی مانند آسیبشناسی سرطان، پیشبینی تخمکگذاری، تجزیهوتحلیل تصویر اشعة ایکس و غیره استفاده شده است.
در مقایسه با انسان، دستگاههای مبتنی بر هوش مصنوعی میتوانند دادهها را با دقت و صحت زیادی تجزیهوتحلیل کنند. بهطور خاص، استفاده از شبکههای عصبی کانولوشن در این دستگاهها، نویدبخش پیشرفت زیادی برای تشخیص بیماریهای مختلف بوده است. CNNها نوعی الگوریتم یادگیری عمیق هستند که میتوانند الگوها را در تصاویر و انواع دیگر دادههای پیچیده تشخیص دهند. محققان بهتازگی، ظرفیت دستگاههای مبتنی بر گوشیهای هوشمند و CNNها را برای تشخیص التهاب ریوی بررسی کردهاند.
بیماری عفونت ریه
پنومونی یا عفونت ریه نوعی بیماری عفونی ریوی است که در بیشتر موارد، علت باکتریایی دارد، اما ممکن است عوامل ویروسی یا بهندرت قارچها نیز در بروز آن نقش داشته باشند. پس از ابتلا، کیسههای هوایی ریه پر از مایع و عفونت میشوند که باعث سرفه همراه با بلغم، چرک، و تبولرز میشود و در نتیجه، تنفس دردناک خواهد شد. ارگانیسمهای مختلفی، مانند باکتری، ویروس، و قارچ، میتوانند سبب التهاب ریه شوند .از طرفی، جذب اکسیژن کاهش مییابد.
بیشتر از همه، سالمندان و کودکان به پنومونی مبتلا میشوند. بیمارانی که دچار ضعف سیستم ایمنی هستند نیز در معرض خطر خواهند بود و در نتیجه، تنفس دردناک خواهد شد. البته، اگر وضعیت بیمار مبتلا به پنومونی طبیعی باشد، بیماری معمولاً پس از دو یا سه هفته، به کمک درمانهای مناسب در منزل، بهبود مییابد. ویروسها و باکتریهای عامل بیماری، از طریق استنشاق هوا یا ذرات عطسه و سرفة بیمار، به فرد دیگری منتقل میشوند.
بهعلاوه، پنومونی در شرایط خاصی مثل تزریق ناسالم مواد، حین بارداری یا پس از تولد نیز ممکن است از طریق خون سرایت کند. در این باره نیز مانند دیگر بیماریهای عفونی، رعایت اقدامات پیشگیرانه مانند شستوشوی مرتب دستها و پوشاندن بینی و دهان هنگام عطسه و سرفه، اهمیت زیادی دارد. در صورت انتقال بیماری در بیمارستان، عفونت بهطور کلی تهاجمیتر و عموماً در برابر آنتیبیوتیک مقاوم خواهد بود. گرچه سیستم دفاعی طبیعی کودکان میتواند با عفونت مقابله کند، کودکانی که ضعف سیستم ایمنی دارند، بسیار بیشتر در معرض خطر ابتلا به پنومونی قرار دارند.
سوءتغذیه از مهمترین علل ضعف سیستم ایمنی کودکان، به خصوص در شیرخوارانی است که بهطور انحصاری با شیر مادر تغذیه نشدهاند. بیماریهای زمینهای مانند آلودگی به ویروس اچآیوی (بهخصوص در نوزادان زیر شش ماه)، سرخک، آنفلوانزا، سرماخوردگی، برونشیت، آسم و ناراحتی های قلبی نیز میتوانند خطر ابتلا را افزایش دهند.
هوش مصنوعی
هوش مصنوعی در سالهای اخیر، در پر کردن شکاف بین تواناییهای انسان و ماشین، رشد بسیار زیادی داشته است. پیشرفتهای حاصلشده در بینایی کامپیوتری با ظهور یادگیری عمیق در طول زمان ایجاد و کامل شده و در درجة اول، بر مبنای الگوریتم خاصی به نام شبکة عصبی پیچشی بوده است. در شبکة عصبیCNN ، ابتدا مرحلة استخراج ویژگی انجام میشود. در این مرحله، هر عکس ورودی از چندین سری لایة کانولوشن و تابع فعالساز ReLU و لایة pooling عبور میکند. سپس عکسهای ورودی به طبقهبندی وارد میشوند. در این مرحله، ابتدا مسطحسازی صورت میگیرد و سپس به لایة Fully Connected وارد میشوند و درنهایت، تابع سافت مکس برای مسائل طبقهبندی چندکلاسه یا تابع سیگموید برای مسائل طبقهبندی باینری، روی آن اعمال میشود تا عکسها بر اساس مقادیر احتمالی، میان صفر و یک طبقهبندی شوند.
مطالعات اخیر
با استفاده از هوش مصنوعی، بیماریهای مرتبط با ریه در چندین مطالعه طبقهبندی و شناسایی شدهاند. ، آیکانات و همکارانش با استفاده از گوشی پزشکی الکترونیکی، روشی غیرتهاجمی برای طبقهبندی صداهای تنفسی ابداع کردند. آنها در مطالعة خود دریافتند که CNNها و ماشینهای بردار پشتیبان ، صداهای تنفسی را بهدقت طبقهبندی میکنند.
چن و همکارانش از طریق استفاده از تصاویر CT با وضوح بالا و یادگیری عمیق، مدلی برای تشخیص بیماری کرونا توسعه دادهاند. عملکرد مدل یادگیری عمیق با رادیولوژیستهای خبره قابل مقایسه بود و در نتیجه، کارایی بالینی رادیولوژیستها را بهبود بخشید.
در این مطالعه، هدف این است که چهارچوب هوش مصنوعی مبتنی بر گوشیهای هوشمند، برای ردیابی التهاب ریوی در مواردی که کووید19 وجود دارد، معرفی شود که از تجزیهوتحلیل الگوی سرخسی نمونههای خلط خشکشده در هوا و دستگاه میکروسکوپ ارزانقیمت و سازگار با گوشیهای هوشمند برای نیل به این هدف استفاده میکند. این بررسی نمایش پلتفرمی با قدرت شبکة یادگیری عمیق در دسترس را برای تشخیص التهاب تنفسی، بدون نیاز به زیرساخت CT یا تجزیهوتحلیل نمونة گسترده ارائه میکند.
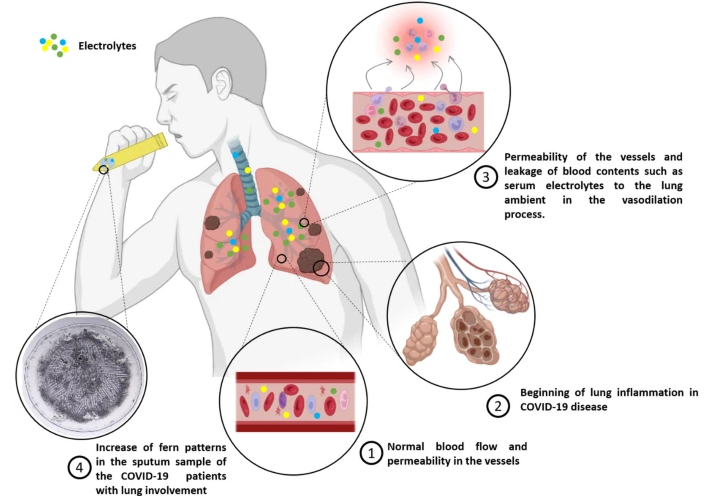
رویکرد ما میتواند به غربالگری سریع بیماران کووید19 برای تعیین شدت بیماری و نیاز به مداخله کمک کند. در مرحلة ایمونولوژیک کووید19، ریهها ملتهب میشوند؛ زیرا سلولهای ایمنی با ویروس مبارزه میکنند. در حال حاضر، سیتیاسکن قفسة سینه چنین التهابی را تشخیص میدهد. این حالت ملتهب اجازه میدهد تا اجزای خون مانند الکترولیتها، در خلط بیمار ظاهر شوند. بنابراین، افزایش نشانگرهای خون در ترشحات تنفسی ممکن است نشاندهندة التهاب ریه باشد.
مایعات بدن، بهویژه خون، علاوه بر اهداف درمانی، مدتهاست که شاخصهای تشخیصی را ارائه کردهاند. باوجود استفاده از بزاق برای تشخیص کووید۱۹، هیچ رویکرد یادگیری عمیق به کمک گوشی هوشمند از افزایش الکترولیتهای خلط برای ردیابی التهاب کووید۱۹ استفاده نکرده است. این قابلیت میتواند غربالگری را برای درگیری شدید ریه بهبود بخشد.
این مطالعه از نمونة خلط بیمارانی که سیتیاسکن ریة آنها مثبت بود، بهعنوان شاخص التهاب ریوی استفاده کرده است. ما الگوهای سرخسی خلط را با استفاده از دستگاه تلفن هوشمند مقرونبهصرفه، ساده و قابل حمل بررسی کردیم. در نمونة خلط کووید19 با اندازة 10 میکرولیتر از بیماران CT مثبت، این الگوها بهعنوان نشانگرهای زیستی التهاب در نظر گرفته شدند. ابتدا، افزایش الکترولیتهای خلط (سدیم، پتاسیم) در بیماران مبتلا به ویروس کووید19 با استفاده از تجزیهوتحلیل استاندارد تأیید شد که با فرضیة نفوذپذیری عروق ما منطبق است.
در مرحلة بعد، ارزیابی مبتنی بر هوش مصنوعی تصاویر ضبطشده با گوشیهای هوشمند، نشان داد که این رویکرد در بیماران مبتلا به ویروس کووید19، توانسته است160 تصویر نمونه خلط بیمار را با دقت 95 درصد در مقایسه با علائم التهابی سیتی اسکن، تشخیص دهد. این روش فشرده و کمهزینه، میتواند به غربالگری هرگونه بیماری التهابی ریه مانند کووید19 کمک کند.
جمعآوری داده و روشهای مورد استفاده
بیماران مبتلا به ویروس کووید-19، که به درگیری ریوی مشکوک بودند و پزشکانشان آنها را برای تصویربرداری CT ریه ارجاع داده بودند، انتخاب و بر اساس نتایج CT مثبت و منفی به دو گروه تقسیم شدند. نمونههای خلط از هر دو گروه جمعآوری شد که در مجموع، شامل هفتاد شرکتکننده بود و همة آنها بهدرستی از روند انجام مطالعه مطلع شدند و رضایت خود را برای این تحقیق ارائه دادند.
جمعآوری خلط کووید19 اول صبح انجام شد و داوطلبان ناشتا بودند و افراد با سابقة مصرف دخانیات و الکل از گروه حذف شدند. پس از جمعآوری، خلط به مدت سی دقیقه دستنخورده باقی ماند. بخشی از خلط جمعآوریشده برای اندازهگیری الکترولیت استفاده شد و حجم کمی (10 میکرولیتر) روی سطح یک لام نمونه قرار گرفت و در دمای اتاق برای خشکشدن باقی ماند. پس از آن، نمونة خشکشده برای ثبت الگوهای سرخس در میکروسکوپ کوچک قرار داده شد و سپس با استفاده از هوش مصنوعی، تجزیهوتحلیل شد.
توسعة الگوریتم هوش مصنوعی
برای تشخیص الگوهای سرخس در بزاق در گوشی هوشمند، از معماری EfficentNet-B0 استفاده شد. برای دستیابی به این کارایی، EfficentNet-B0 از روش مقیاسبندی ترکیبی برای تنظیم همزمان عمق، عرض و وضوح آن استفاده میکند. با استفاده از این روش، میتوان تصاویر را با دقت بیشتری با پارامترهای کمتر طبقه بندی کرد و در نتیجه، نمایشهای پیچیدهتری به وجود آورد. EfficientNet-B0 یک معماری است که ۳/۵ میلیون پارامتر قابل آموزش دارد.
چنین شبکة عصبی پیچیدهای برای بهینهسازی پارامترهای خود در حین آموزش، به تعداد قابل توجهی تصویر نیاز دارد که از مجموعة ImageNet، که یک مجموعه داده شامل چهارده میلیون تصویر طبقهبندیشده از دستههای مختلف است، استفاده کرده است. مدل از پیش آموزشدیده شده، با استفاده از مجموعهدادههای شامل 650 تصویر بزاق گرفتهشده از 70 شرکتکننده، که به گروههای سرخس و غیرسرخس طبقهبندی شدهاند، اعتبارسنجی شد.
مجموعه دادههای برچسبگذاریشده 80 درصد به 20 درصد برای آموزش و ارزیابی تقسیم شدند که 520 نمونه مربوط به آموزش دادهها و 130 نمونه برای بخش ارزیابی اختصاص داده شد. پیش پردازش تصاویر و تغییر اندازة تصاویر به ابعاد 224×224 پیکسل قبل از ورود آنها به شبکه عصبی انجام میشود. دومین بخش طبقهبندی است. الگوریتم بهینهسازی انتخابشده RMSProp است که برای بهحداقلرساندن تابع آنتروپی متقابل استفاده میشود.
سیستم ایمنی به بسیاری از گلبولهای سفید خون سیگنال میدهد تا به محیط ریه بروند و با ویروسها مبارزه کنند. برای تسهیل این فرایند، ریز رگهای کوچک اطراف آلوئول تنفسی گشاد و نفوذپذیر میشوند و به سلولهای ایمنی اجازة عبور میدهند. افزایش نفوذپذیری عروق به پر شدن کیسههای هوا با مایع خونی منجر و در نتیجه، سندرم دیسترس تنفسی حاد و متعاقب آن، نارسایی ریه در نواحی خاص ایجاد میشود. فرضیة ما بیان میکند که نفوذ سرم خون به محیط ریه، ترکیب و غلظت اجزای خلط، بهویژه نمکهای الکترولیت مانند K و Na را تغییر میدهد.
پس از نتایج CT، بیماران به دو گروه CT مثبت و CT منفی دستهبندی شدند. سپس نمونههای خلط ناشتا از بیماران جمعآوری شد و دستگاه آنالایزر الکترولیت، یونهای سدیم و پتاسیم آنها را اندازهگیری کرد. سدیم و پتاسیم، الکترولیتهای اولیة سرم خون هستند. افزایش قابل توجهی از غلظت سدیم و پتاسیم در نمونههای خلط بیماران CT مثبت قابل مشاهده است.
میانگین غلظت سدیم و پتاسیم در نمونههای CT منفی تقریباً 29 میلیمول در لیتر و 26 میلیمول در لیتر است، درحالیکه این مقادیر در موارد CT مثبت به حدود 53 میلیمول در لیتر و 46 میلیمول در لیتر میرسد. این یافتهها این فرضیه را تأیید میکنند که الکترولیتهای آزادشده در سیستم تنفسی، بهدلیل التهاب و متعاقب آن گشادشدن عروق، میتوانند در نمونههای خلط شناسایی شوند.
بحث و نتیجهگیری
این مطالعه روش جدیدی معرفی کرده است که میتواند در تشخیص درگیری ریوی و التهاب ریه در بیماران مبتلا به بیماریهایی مانند کرونا کمککننده باشد. این روش برای دیگر بیماریهای ریوی مانند آسم، COPD و غیره اعمال نشده است. بااینحال، با توجه به مکانیسمهای مشابه آنها با کووید-19، پیشبینی میکنیم این سیستم برای آنها نیز عملکرد مشابهی داشته باشد.
این سیستم شامل مینی میکروسکوپ قابل حمل و برنامهای مبتنی بر هوش مصنوعی در تلفن هوشمند برای تشخیص الگوهاست. برای تأیید فرضیه دربارة ورود الکترولیتهای سرم به خلط در مرحلة التهابی بیماری، ابتدا غلظت الکترولیت (سدیم و پتاسیم) در نمونههای خلط هر دو مورد CT مثبت و CT منفی اندازهگیری شد. در نهایت، نتایج فرضیة ما ثابت کرد که میزان الکترولیت در خلط بیماران CT مثبت بیشتر است. ساختار سرخس به کمک مینی میکروسکوپ با کمک گوشی هوشمند و برنامهای مبتنی بر هوش مصنوعی ارزیابی شد. تصاویر به اپلیکیشنی در گوشی هوشمند ارسال میشود تا با استفاده از CNN آنالیز شود و الگوهای سرخس در خلط را بهعنوان نشانهای از التهاب ریوی تشخیص دهد.
منبع
1. Ghaderinia, M & Abadijoo. H. (2024), “Smartphone-Based Device for Point-of-Care Diagnostics of Pulmonary Inflammation Using Convolutional Neural Networks (CNNs)”, Scientific Reports, vol. 14: 6912.
تهیهوتنظیم: دکتر ندا کفاش